Ionebinding, også kjent som ionisk binding, er en grunnleggende konsept innen kjemi som spiller en viktig rolle i å danne og opprettholde stabile forbindelser. I denne artikkelen vil vi utforske hva en ionebinding er, hvordan den dannes, og hvilke karakteristiske egenskaper den har. Gjennom en informativ og nøytral tilnærming vil vi forklare denne kjemiske bindingstypen i detalj og forhåpentligvis øke din forståelse og kunnskap innenfor dette feltet.
Definisjon og forklaring av en ionebinding
En ionebinding er en type kjemisk binding som oppstår mellom to atomer ved at de deler eller overlapper elektroner. Ionebinding oppstår mellom en positivt ladet ion og en negativt ladet ion, og er vanligvis sett mellom et metall og et ikke-metall i et salt. Denne typen binding er svært sterk og fører til dannelse av en krystallinsk struktur.
I en ionebinding overføres elektroner fra et atom til et annet. Det atom som avstått elektronet blir positivt ladet, og danner en positivt ladet ion (kation), mens det atom som har mottatt elektronet blir negativt ladet og danner en negativt ladet ion (anion). Disse motsatte ladningene tiltrekker hverandre og danner dermed en stabil binding.
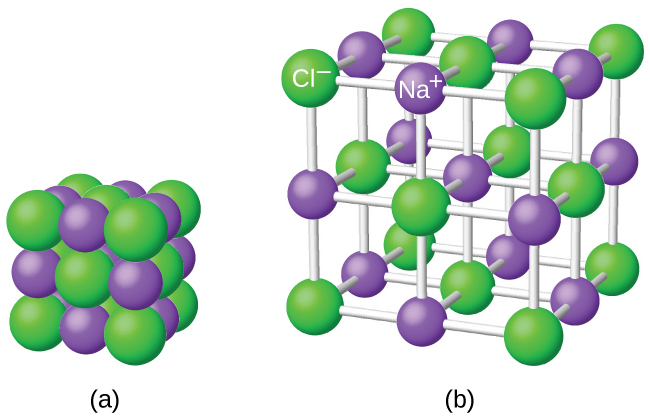
Eksempel på en ionebinding er natriumklorid (NaCl), der natriumatomet har avstått et elektron til kloratomet. Dette resulterer i dannelse av natriumionet (Na+) og kloridionet (Cl-), og disse ionene tiltrekker hverandre og danner en krystallinsk struktur. Ionebindinger er ansvarlige for egenskapene til mange kjemiske forbindelser og er viktige for å opprettholde struktur og stabilitet i ulike materialer.

Egenskaper og struktur av ioniske forbindelser
En ionebinding er en type kjemisk binding som dannes mellom to ioner med motsatt ladning. Denne typen binding oppstår vanligvis mellom et positivt ladet metallion og et negativt ladet ikke-metallion. Ionene blir dannet når atomer mister eller får elektroner for å oppnå en stabil elektronkonfigurasjon.
Ionebindinger har flere karakteristiske egenskaper og strukturer. Først av alt, på grunn av elektrostatisk tiltrekning mellom de motsatte ladningene, har ioniske forbindelser generelt høy smelte- og kokepunkt sammenlignet med molekylære forbindelser. Dette skyldes den sterke bindingen mellom atomene i ionene.
I tillegg har ioniske forbindelser vanligvis en krystallinsk struktur, som er veldig regelmessig og ordnet. Dette skyldes at ionene ordner seg i et gittermønster for å maksimere den elektrostatiske tiltrekningen mellom dem. Denne strukturen resulterer i sterke bindinger og høy stabilitet i ioniske forbindelser. Et eksempel på en ionisk forbindelse er natriumklorid (NaCl), der natriumioner (Na+) og klorioner (Cl-) danner et tredimensjonalt krystallgitter.
Sammensetning, egenskaper og anvendelser av typiske eksempler på ionebindinger
Ionebindinger er en type kjemisk binding som oppstår mellom et metall og en ikke-metall. Denne typen binding dannes når elektroner overføres fra ett atom til et annet, og resulterer i dannelse av positivt og negativt ladde ioner. Det positive ionet dannes når atomet gir fra seg elektroner, og det negative ionet dannes når atomet mottar elektroner. Disse motstridende ladningene tiltrekker hverandre og danner en sterk kjemisk binding.
En av de vanligste eksemplene på ionebinding er dannelsen av natriumklorid (NaCl). Her vil natriumatomet gi fra seg ett elektron til kloratomet, som resulterer i dannelse av Na+-ioner og Cl–ioner. Disse ionene tiltrekker hverandre på grunn av de motsatte ladningene, og danner dermed en stabil krystallstruktur. Ionebindinger er generelt sett svært sterke og har høy smelte- og kokepunkt på grunn av den sterke tiltrekningen mellom ionene.
Ionebindinger har mange anvendelser og er viktige i mange kjemiske og industrielle prosesser. De brukes for eksempel i produksjon av mineralgjødsel, der ionebindinger er nødvendige for å skape næringssalter som plantene kan absorbere. Ionebindinger er også avgjørende for dannelsen av saltkrystaller, som brukes i matlaging, kjemisk industri og medisinske applikasjoner. I tillegg spiller ionebindinger en stor rolle i dannelse av salter i havvann og ferskvann, som har betydning for økosystemene og marine livsformer. Et annet eksempel er dannelse av kalkstein, der ionebindinger er ansvarlige for å binde sammen kalsium- og karbonationer for å danne det faste stoffet. Til slutt har vi kommet til enden av vår forklaring på hva en ionisk binding er. Vi har utforsket de grunnleggende begrepene og prinsippene som ligger bak dette viktige kjemiske fenomenet. Gjennom artikkelen har vi sett hvordan atomer kan miste eller få elektroner, og hvordan disse ionene tiltrekker seg hverandre for å danne stabile forbindelser.
Vi har forstått at ioniske bindinger dannes mellom positive og negative ioner, og at elektrostatiske krefter spiller en nøkkelrolle i å opprettholde strukturen til disse forbindelsene. Ved å studere eksempler som natriumklorid og magnesiumoksid har vi sett hvordan ioniske bindinger gir opphav til karakteristiske egenskaper som høy smelte- og kokepunkt, samt god elektrisk ledningsevne i smeltet form.
Vi håper denne artikkelen har hjulpet deg med å forstå hva en ionisk binding er og hvordan den påvirker kjemiske reaksjoner og egenskapene til stoffer. Ioniske bindinger er avgjørende for å forstå sammensetningen og atferden til en rekke naturlige og kunstige materialer.
Husk at ioniske bindinger er bare en del av den komplekse verdenen av kjemi og at det er mye mer å utforske. Fortsett å dypdykke i dette spennende fagfeltet for å utvide kunnskapen din om molekyler, bindinger og interaksjoner på atomnivå. Med en solid forståelse av ioniske bindinger vil du kunne forstå en verden av kjemiske reaksjoner som ligger bak alt fra hverdagslige hendelser til store industrielle prosesser.
Vi håper du har funnet denne artikkelen informativ og nyttig. God utforskning av kjemien verden!